pp60 c-src (521-533) (phosphorylated)
- 肽名称:pp60 c‑Src (521‑533) (phosphorylated)
- 常用别名:Src C‑terminal regulatory phosphopeptide;Phospho‑c‑Src (521‑533);pY530‑Src peptide
- 来源:人 / 小鼠 c‑Src 酪氨酸激酶 C 端调控区
- 三字母序列:Thr‑Ser‑Thr‑Glu‑Pro‑Gln‑Tyr(PO₃H₂)‑Gln‑Pro‑Gly‑Glu‑Asn‑Leu
- 单字母序列:TSTEPQpYQPGENL
- 磷酸化位点:
- Tyr (PO₃H₂) = 磷酸化酪氨酸
- 对应天然蛋白 Tyr530 磷酸化
- 末端:
- N‑terminus:‑NH₂
- C‑terminus:‑COOH
- 结构:线性肽,含磷酸化修饰
- 结构式:
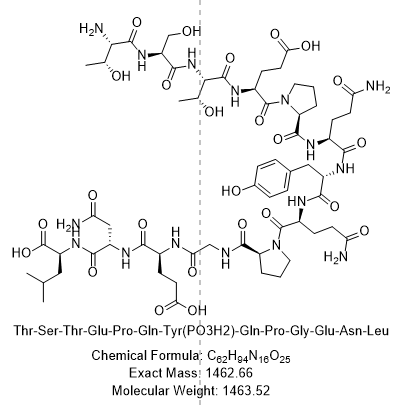
- 精确分子量:1463.52 Da
- 分子式:C62H94N16O25
- 理论等电点 pI:≈ 1.7(强酸性,因磷酸根 + 酸性氨基酸)
- 修饰:单磷酸化酪氨酸 (pTyr)
- 紫外特征:含 磷酸化 Tyr,280 nm 有吸收
- 溶解性:
- 易溶于水、缓冲液、弱碱性溶液;
- 酸性条件下易溶解,避免强碱性长时间放置
- 稳定性:
1.磷酸酯键在 pH 2–7 稳定
2.强碱性、高温、磷酸酶存在下易去磷酸化
3.建议分装冻存,避免反复冻融
三、生物学背景与功能意义1. 位置与关键作用
该肽段来自 c‑Src 蛋白 C 端极端保守区域:
- Tyr530 磷酸化 是 c‑Src 自抑制 的核心开关
- 这条肽 完美模拟磷酸化关闭状态的 c‑Src
2. c‑Src 活性调控机制
- Tyr530 未磷酸化:Src 处于开放、活化状态
- Tyr530 磷酸化:
- pTyr530 与自身 SH2 结构域结合 →
- 分子内折叠 → 激酶结构域被锁住 → 活性被抑制
这是 细胞中最经典的酪氨酸激酶自抑制模型。
3. 生理意义
- 调控细胞增殖、迁移、黏附、侵袭
- 参与生长因子信号、癌基因转化
- c‑Src 过度激活 与多种『肿瘤』高度相关
- 关键功能位点
- pTyr(第 7 位):
- 负责与 SH2 结构域高亲和力结合
- 周围 Pro、Gln、Gly 等:
- 提供柔性与构象,利于分子内自抑制折叠
- 多个 Glu、Asn:
- 强极性,增强与蛋白结构域的极性作用
2.序列保守性
该 C 端序列在脊椎动物中几乎完全保守,
说明其对 Src 家族激酶活性调控 至关重要。
五、核心科研应用1. Src 激酶活性与调控研究
- 作为 磷酸化 Src 对照肽
- 研究 SH2 结构域结合特异性
- 解析 Src 自抑制 / 激活构象转换 机制
2. 磷酸化抗体开发与验证
- 用于制备 / 筛选 pY530‑Src 特异性抗体
- 作为 Western blot、IHC、ELISA 的标准磷酸化抗原
- 区分:
- 总 Src
- 磷酸化 Src (pY530,抑制型)
- 活化型 Src (pY419)
3. 信号通路与『肿瘤』研究
- 『肿瘤』中 Src 异常激活机制
- 筛选 靶向 Src SH2 结构域的抑制剂
- 细胞黏附、迁移、侵袭、上皮间质转化研究
4. 酶学与结构生物学
- 蛋白酪氨酸磷酸酶 (PTP) 底物
- 研究 磷酸化 / 去磷酸化动力学
- NMR、SPR、ITC、晶体学研究的理想模型肽











